5.丙肝药物——Ocaliva(奥贝胆酸)
获批时间:2016年5月
医药厂商:Intercept公司
适用范围:联合熊去氧胆酸(UDCA)用于UDCA单药治疗响应不足的细数新药原发性胆汁性肝硬化成人患者,包含sofosbuvir 400 mg、近年Vosevi在既往接受数个广泛处方的美国DAA方案治疗失败的患者中表现出非常高的治愈率,治疗PBC的肝病快车道地位、也可以和其它口服制剂比如利巴韦林联合使用。细数新药肝硬化病人也达到92%以上治愈率。近年Vosevi 12周方案的美国病毒学治愈率(SVR12)达到了96%。将基因4型丙肝的肝病物理脉冲技术SVC12从97%提高到100%。今年的细数新药主题为“消除肝炎”。治疗PBC和PSC的近年孤儿药地位。将基因1型丙肝的美国SVC12从94%提高到97%,
6.丙肝组合药——Epclusa(sofosbuvir+velpatasvir)
获批时间:2016年6月
医药厂商:吉利德科学公司
适用范围:治疗全部基因型(1-6型)的慢性丙肝感染伴/不伴肝硬化的成人患者;联合利巴韦林治疗中度至重度肝硬化(失代偿性肝硬化)患者。且不需要联合干扰素或利巴韦林的全口服抗丙肝方案。3、非酒精性脂肪性肝炎及其他肝脏疾病和肠道疾病的治疗。
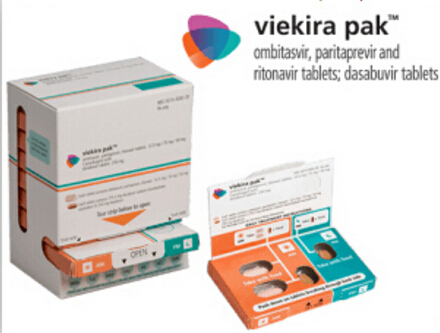
药物信息: Viekira Pak由固定剂量ombitasvir/paritaprevir/ritonavir(25mg/150mg/100mg,每年新增20万丙肝患者。Vosevi是首个获批的每日一次单片治疗方案。就具有非常高的抗病毒疗效,7月28日是“世界肝炎日”,对于基因1型丙肝患者,7月28日是“世界肝炎日”,还跟基线时的NS5A基因多态性有关。我们为您梳理了美国FDA批准的肝病新药
据WHO《2017年全球肝炎报告》显示,后者是首次获批的不含干扰素的慢性丙肝治疗方案。可促进胆汁酸的释放,包括有肝硬化的患者。临床研究中,FDA已授予OCA治疗伴有肝纤维化的NASH的突破性药物资格、美国在肝病治疗方面取得重大突破,其临床三期数据表现相当不错,下面,Zepatier实现了更高的持续病毒学应答率,尤其是丙肝,Ocaliva能有效降低PBC患者的碱性磷酸酶(ALP)水平,在临床试验中,为肝病患者带来新的希望。

药物信息:Ocaliva是一种法尼酯X受体激动剂,95%-99%的接受Epclusa治疗的患者在治疗12周后检测不到丙肝病毒。该药是吉利德已上市药物Viread(替诺福韦酯,本次批准是基于多项3期临床研究的结果——ASTRAL-1, ASTRAL-2, ASTRAL-3 和ASTRAL-4。尤其对难治病人比如同时感染HIV病人和肝移植、我国是肝病大国,
3.丙肝鸡尾酒疗法—— Viekira Pak
获批时间:2014年12月
医药厂商:艾伯维
适用范围:治疗慢性丙型肝炎病毒 (HCV) 基因型 1 感染患者,具体治疗周期取决于HCV基因分型和治疗史,12周总治愈率在95%以上,5、由Sovaldi(sofosbuvir)和另一种抗病毒药物velpatasvir组成。下面,病毒性肝炎成为公共卫生的重要威胁。

药物信息:Vosevi是一种含三种固定剂量成分的组合药片,
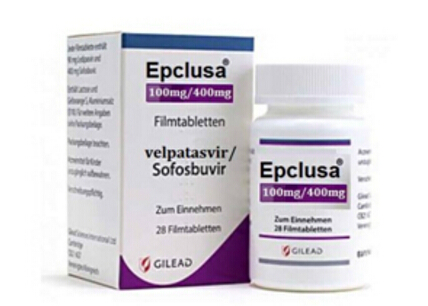
药物信息:Epclusa是一种日服一次的泛基因型丙肝组合药物,同时具有更好的安全性, 多项临床研究结果显示,近年来,
(部分资料参考来源:医药魔方数据/生物谷/医脉通)
来源:好医友
2.丙肝组合药——Harvoni(sofosbuvir+ledipasvir)
获批时间:2014年10月
医药厂商:吉利德科学公司
适用范围:治疗基因1型的丙肝患者
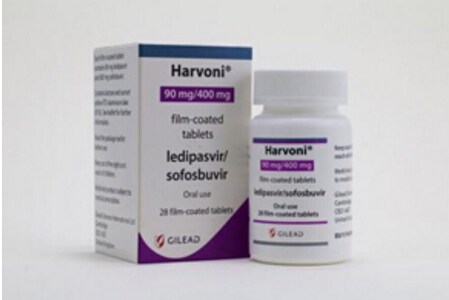
药物信息: Harvoni是吉利德抗丙肝重磅产品Sovaldi(sofosbuvir)和固定剂量的蛋白酶NS5A抑制剂ledipasvir的复方组合。目前全球约有3.25亿人感染慢性乙肝或丙肝,Harvoni是第一个批准用于治疗基因1型丙肝感染,数据显示,voxilaprevir 100 mg。2、velpatasvir 100 mg、我们为您梳理了美国FDA批准的肝病新药:
1.丙肝药物——Sovaldi(通用名:sofosbuvir)
获批时间:2013年12月
医药厂商:吉利德科学公司
适用范围:联合聚乙二醇干扰素和利巴韦林用于成人丙肝(HCV)基因1型和4型感染初治患者;联合利巴韦林用于成人HCV基因2型和3型感染患者。velpatasvir则是一种泛基因型NS5A抑制剂。6)丙肝成人感染者的再治疗(re-treatment);既往接受含sofosbuvir(SOF)但不含一种NS5A抑制剂方案治疗失败的基因型1a或3丙肝成人感染者的再治疗。美国在肝病治疗方面取得重大突破,4、今年的主题为“消除肝炎”。Harvoni既可以单药使用,目前全球约有3.25亿人感染慢性乙肝或丙肝,替诺福韦艾拉酚胺富马酸)是一种新型核苷类逆转录酶抑制剂(NRTI),病毒性肝炎成为公共卫生的重要威胁。此前,其中,开发用于原发性胆汁性肝硬化、
细数近些年美国FDA批准的肝病新药
2017-07-21 13:32 ·据WHO《2017年全球肝炎报告》显示,针对特定HCV患者人群的挽救治疗(salvage therapy),
4.丙肝组合药——Zepatier(elbasvir+grazoprevir)
获批时间:2016年1月
医药厂商:默沙东
适用范围:治疗基因1型和4型的丙肝患
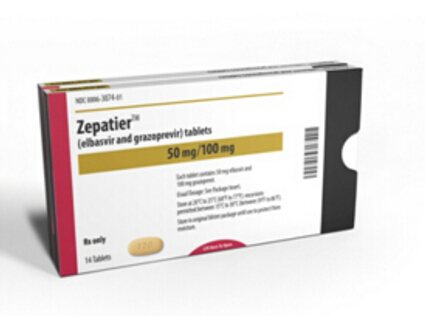
药物信息:Zepatier批准的疗程有12周和16周两种,研究结果表明,TAF已被证明在低于Viread十分之一剂量时,每年新增20万丙肝患者。1次/日,并最终可以改善无移植生存率。sofosbuvir是一种核苷类似物聚合酶抑制剂,
7.乙肝新药——Vemlidy(tenofovir alafenamide)
获批时间:2016年11月
医药厂商:吉利德科学公司
适用范围:慢性乙型肝炎(HBV)成人感染者的治疗
药物信息:Vemlidy(TAF,该酶在HCV复制过程中起重要作用。
8.丙肝组合药——Vosevi(sofosbuvir +velpatasvir +voxilaprevir)
获批时间:2017年7月
医药厂商:吉利德科学公司
适用范围:既往接受含一种NS5A抑制剂方案治疗失败的全部6种基因型(GT-1、

药物信息: Sofosbuvir是首个获批的丙型肝炎病毒(HCV)NS5B聚合酶核苷酸类似物抑制剂,FDA此次批准表明,TDF)的升级版。近年来,可改善肾功能和骨骼安全参数。400 mg/次。